Das Ende der modernen Medizin?
Antibiotika sind Wunderwaffen. Doch gegen immer mehr Keime wirken sie nicht mehr. Jetzt droht der Super-GAU.

MRSA: Der multiresistente Staphylococcus aureus. 30 Prozent der Menschen tragen den meist harmlosen Keim in Nase und Haut. Bei geschwächter Immunabwehr können Geschwüre, Blutvergiftung und Lungenentzündung auftreten.
Bakterien sind Könige. Sie machen sich in allen Winkeln und Ritzen unseres Planeten breit und besiedeln erfolgreich Pflanzen, Tiere und Menschen – manchmal als Krankheitserreger. Bakterien sind überdies schlau: Sie kennen viele Tricks, um sich gegen Angreifer zu behaupten.
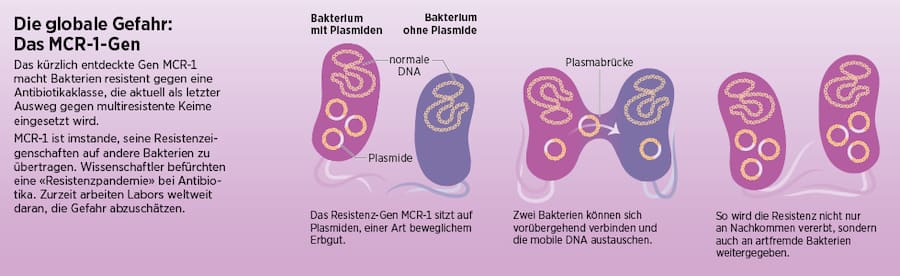
Raffiniert ist zum Beispiel das Molekül MCR-1. Es hält die Fachwelt in Aufruhr, seit das Fachmagazin «Lancet: Infectious Diseases» im November über das kleine Monster berichtet hat. Forscher in China haben es in Darmbakterien von Schweinen und Hühnern entdeckt. MCR-1 ist ein Resistenz-Gen, das anders agiert als die bisher bekannten: Es verbreitet seine Eigenschaften nicht über den schwerfälligen Weg natürlicher Auslese, sondern sitzt ausserhalb des Bakterienchromosoms in einem Plasmid. Plasmide sind ringförmige DNA-Moleküle, die wie Legosteinchen im Bakterium sitzen. Sie können andere Bakterien effizient mit ihrer Erbinformation anstecken, auch solche einer völlig anderen Spezies.
Das Perfide an MCR-1: Es macht Bakterien unempfindlich gegen Colistin, das «letzte» Reserveantibiotikum, das Ärzte bei Infektionen einsetzen, wenn alle anderen versagen. Seit 1959 auf dem Markt, wird Colistin nur im äussersten Notfall angewendet, da es schwere Nebenwirkungen hat und Nierenschäden verursachen kann. Nun setzt MCR-1 die letzte antibiotische Verteidigung ausser Gefecht.
Für die Medizin sind das schlechte Neuigkeiten. «Dieses MCR-1-Gen macht uns etwas Angst, weil es sich mit resistenten Keimen koppeln könnte, die den Spitälern jetzt schon grosse Sorgen bereiten», sagt Rein Jan Piso, Chef-Infektiologe am Kantonsspital Olten. Andreas Widmer, Leiter Spitalhygiene am Universitätsspital Basel, sieht gar das «postantibiotische Zeitalter» angebrochen. «Wenn Patienten mit resistenten Keimen besiedelt sind und alle Antibiotika versagen, können wir zum Beispiel keine Organtransplantationen mehr sicher durchführen», sagt der Präsident der Expertengruppe Swissnoso, die sich Spitalinfektionen und multiresistenten Keimen im Gesundheitswesen widmet.
Äusserst besorgt ist auch die Weltgesundheitsorganisation (WHO). Deren Generaldirektorin Margaret Chan sprach angesichts zunehmender Antibiotikaresistenzen unlängst von einer «globalen Gesundheitskrise», die beängstigende Ausmasse angenommen habe.
Die Autoren der «Lancet»-Studie orteten den Ursprung von MCR-1 im Perlflussdelta im Süden Chinas, einer Region, die sich innert weniger Jahrzehnte vom schwach entwickelten Agrarraum zur pulsierenden, schnell wachsenden Wirtschaftszone gewandelt hat. Die Forscher analysierten Schweine- und Geflügelproben, die sie auf traditionellen Tiermärkten und in den modernen Konsumtempeln der 14-Millionen-Stadt Guangzhou (Kanton) erworben hatten.
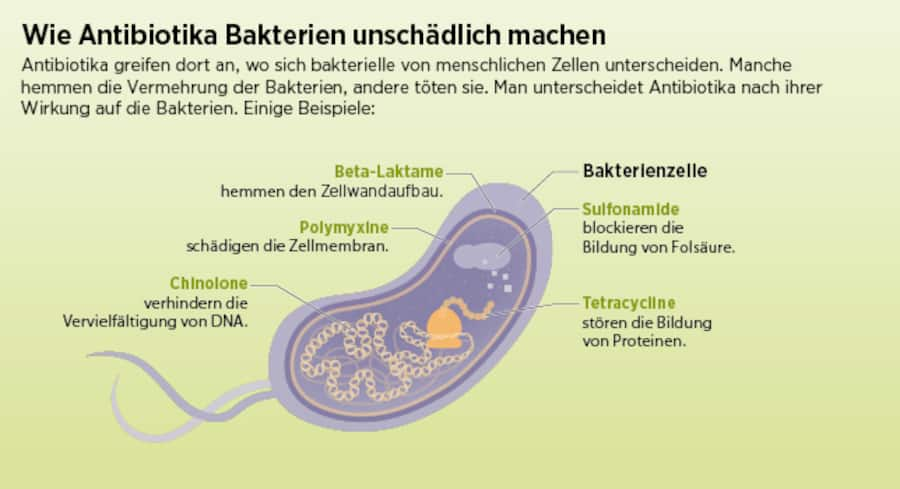
In den immensen Tierfabriken der Provinzen hatten sie beobachtet, dass die Schweine und Hühner routinemässig grosse Mengen des Antibiotikums Colistin als Wachstumsförderer zu fressen bekamen – eine Praxis, die in der Schweiz und der EU verboten ist. Die Wissenschaftler stellten fest, dass die Darmbakterien E. Coli der Tiere zu beträchtlichen Anteilen unempfindlich waren gegen Colistin. Auch in Stuhlproben von Spitalpatienten entdeckten sie Bakterienstämme mit dieser Resistenz.
«Wissenschaftler vermuteten seit langem», schrieb die britische «Sunday Times», «dass der Süden Chinas mit seiner Mischung von Millionen Menschen und Tieren, den unhygienischen Lebensbedingungen, dem subtropisch-feuchten Monsunklima und den keimbelasteten Gewohnheiten und Bräuchen – vom Spucken auf der Strasse bis zum Trinken von Entenblut als Delikatesse – eine Brutstätte für globale Krankheiten ist.» Die Forscher ihrerseits mahnten, noch sei MCR-1 auf China begrenzt, aber es sei nur eine Frage der Zeit, dass sich das Resistenz-Gen global verbreite.
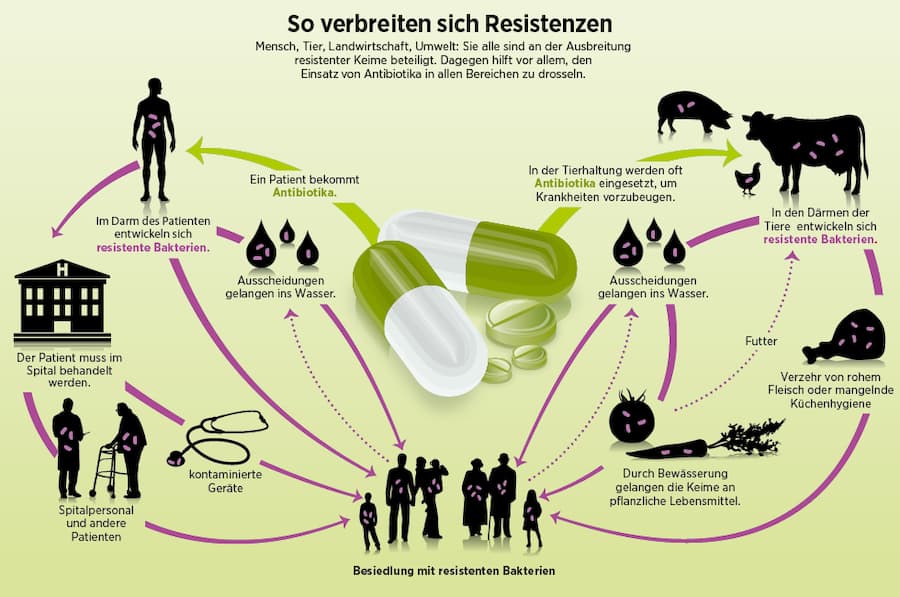
Inzwischen weiss man: Das ist längst geschehen. Und möglicherweise ist China gar nicht der Ursprung von MCR-1, sondern lediglich das Land, in dem die Resistenz erstmals entdeckt wurde. Seit Erscheinen des «Lancet»-Papers im November suchen Wissenschaftler rund um den Globus fieberhaft nach MCR-1, ein regelrechtes Wettrennen um neue Nachweise ist entbrannt. Mit dabei an vorderster Front ist die Schweiz: Lebensmittelwissenschaftler der Uni Zürich haben die Resistenz bei E.-Coli-Stämmen aus einheimischem Flusswasser sowie aus importiertem Gemüse und Geflügel entdeckt (siehe Interview mit Veterinärmediziner Roger Stephan).
Nicht minder aktiv ist die Gruppe um den Mikrobiologen Patrice Nordmann an der Uni Freiburg, die MCR-1 ebenfalls in verschiedenen Bakterienstämmen nachgewiesen hat, darunter in Tierproben aus Frankreich, England und Dänemark. Die älteste Probe ist aus dem Jahr 2005 und stammte von einem Kalb in Frankreich.
Aber auch hierzulande ist MCR-1 bereits in einem Spital aufgetaucht. Nordmanns Gruppe entdeckte das Gen in einem Bakterienstamm aus einer Urinprobe eines 83-jährigen Patienten, der im Dezember letzten Jahres wegen entzündeter Darm-Ausstülpungen hospitalisiert worden war. Besonders beunruhigend: Die isolierten E.-Coli-Bakterien des Mannes waren nicht nur resistent gegen Colistin, sondern gegen eine ganze Reihe weiterer Reserveantibiotika, die sogenannten Carbapeneme. «Es ist völlig unklar, wo der Mann den gefährlichen Keim aufgelesen hat, denn er war seit geraumer Zeit nicht ins Ausland gereist», sagt Patrice Nordmann. Glücklicherweise hatten die Ärzte in diesem Fall noch ein Medikament in petto, so dass der Patient trotzdem behandelt werden konnte.
Seit ihrer Entdeckung vor über 70 Jahren sind Antibiotika die wichtigste Waffe, um bakterielle Infektionen wirksam zu behandeln. «Es war Zufall, dass der schottische Bakteriologe Alexander Fleming 1928 das Penicillin entdeckte», erzählt der Oltner Infektiologe Rein Jan Piso. Aus der Luft waren Sporen von Schimmelpilzen auf die Platte gelangt, auf der Fleming Staphylokokken anzüchtete. Diese waren im Umkreis der Schimmelpilze sozusagen aufgelöst. Fleming gelang es, den dafür verantwortlichen Stoff zu isolieren – und nannte ihn Penicillin.
Anfang der vierziger Jahre schafften es andere Forscher, die Substanz in grösseren Mengen herzustellen. Anfänglich als Wunderwaffe gefeiert, verlor Penicillin jedoch bei gewissen Keimen mit der Zeit seine Wirkung. «Man erkannte, dass Bakterien imstande sind, wirksame Gegenmassnahmen gegen das Medikament zu entwickeln», sagt Rein Jan Piso.
Heute sind Antibiotikaresistenzen ein globales Problem, das die öffentliche Gesundheit und die Errungenschaften der modernen Medizin zunehmend bedroht. Schon vor Jahren haben Wissenschaftler und Behörden erkannt, dass es vor allem der übermässige und teils unsachgemässe Gebrauch von Antibiotika ist, der Bakterien resistent werden lässt. Das Bundesamt für Gesundheit schätzt, dass schweizweit jährlich rund 70'000 spitalbedingte Infektionsfälle auftreten, die bei 2000 Patientinnen und Patienten zum Tod führen, und dass ein Teil dieser Infektionen durch resistente Keime verursacht ist. «Deshalb tun wir im Spital das absolut Mögliche, um die Übertragung von Krankheitserregern, neben Bakterien auch Viren, zu verhindern», sagt Infektiologe Piso. Der damit verbundene Aufwand und die erforderliche «Manpower» seien beträchtlich.
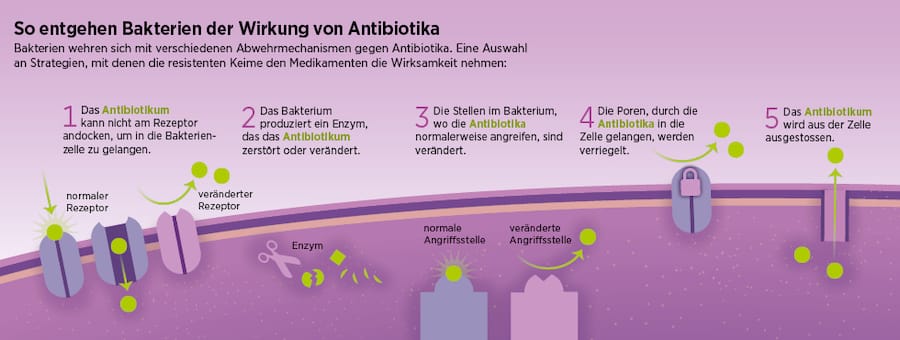
Das ist im Kantonsspital Olten auch für Aussenstehende unübersehbar. Schon am Eingang informiert ein grosses Plakat über die wichtigsten Hygieneregeln – und bittet Besucher, die zum Beispiel an Grippe erkrankt sind, fernzubleiben. An jeder Ecke, in jedem Flur stehen Spender bereit, die mit Piktogrammen zum richtigen Desinfizieren der Hände einladen. Die fürs Personal geltenden Hygienestandards sind umfassend, für Ärzte genauso wie für Pflegende, Reinigungsfachleute oder administrativ Tätige.
Dass sie eingehalten werden, dafür sorgen Hygienespezialistinnen wie Elisabeth Grui: «Achtgeben, was man anfasst, sich die Wege auf der Station gut überlegen und vor allem jedes Mal die Hände desinfizieren, wenn man das Zimmer eines Patienten betritt oder verlässt: Diese Regeln trichtern wir den Angestellten gebetsmühlenartig ein. Denn wenn wir aufhören, von Hygiene zu sprechen, werden die Massnahmen weniger eingehalten.» Ärzte und Pflegende tragen ständig ein Fläschchen mit Desinfektionsmittel auf sich. Unzählige Male pro Tag reiben sie sich die Hände ein. Auch die Reinigung ist elementar. Bestimmte Oberflächen in den Zimmern werden in hoher Frequenz mit wirkungsvollen Desinfektionsmitteln behandelt – Pflegetische, Waschschüsseln, Nachttische, Bettrahmen und so weiter. All diese Massnahmen sollen verhindern, dass Keime übertragen werden.
Zu den Sorgenkindern zählen vor allem multiresistente Bakterien wie MRSA, VRE (siehe Bildergalerie) oder Salmonellen. Aber auch hochinfektiöse Viren wie das Norovirus machen den Spitälern zu schaffen. Elisabeth Grui erzählt, wie sie vor vielen Jahren einmal einen Patienten wegen Noroviren isolieren musste. «Ein Arzt hob die Isolation wieder auf. Darauf steckten sich mehrere Mitarbeiterinnen der Station an. Von da an war meine Arbeit akzeptiert.»
Wenn ein Patient mit einem gefährlichen Erreger infiziert sein könnte, handeln die Spitalverantwortlichen in Olten rasch. «Bei Personen, die in den vorangegangenen sechs Monaten im Ausland im Spital waren, machen wir automatisch einen MRSA-Schnelltest», erklärt Elisabeth Grui.
Bestätigt sich ein Verdacht, wird die betroffene Person in ein Isolationszimmer mit Schleuseneingang verlegt und dort behandelt. Isolation bedeutet: Das Pflegepersonal trägt im Zimmer Schutzkleidung samt Mundschutz und Handschuhen. Die Wäsche des Patienten wird samt dem Wäschebeutel gewaschen. So gelinge es, Infektionen einzudämmen.
Macht nun der MCR-1-Mechanismus all diese Bemühungen zunichte? Stehen wir vor dem «Ende der Antibiotika», wie zu lesen war? Spezialisten wie Patrice Nordmann sind nicht ganz so pessimistisch. «MCR-1 ist eine Bedrohung, zweifellos», sagt der Freiburger Mikrobiologe. «Doch die meisten Bakterienstämme wurden bislang in Tieren und nicht bei Menschen gefunden – das lässt Hoffnung aufkeimen.»
Dazu kommt, dass Wissenschaft und Politik fest entschlossen scheinen, gegen Antibiotikaresistenzen vorzugehen, und zwar in einem ganzheitlichen Ansatz, der alle Akteure einbezieht: Humanmedizin, Tiermedizin, Landwirtschaft und Umwelt.
Im November letzten Jahres hat der Bund die nationale Strategie Antibiotikaresistenzen (Star) lanciert, deren oberstes Ziel es ist, «die Wirksamkeit von Antibiotika für Mensch und Tier langfristig zu erhalten». Und am World Economic Forum im Januar in Davos forderten 85 Pharmakonzerne «in einer beispiellosen Aktion» – wie die Medien jubelten – einen verantwortungsvollen Umgang mit Antibiotika. Es war das erste Mal, dass sich die globale Pharmaindustrie praktisch geschlossen auf eine gemeinsame Erklärung einigte.
Nicht zuletzt kann auch jede Einzelne und jeder Einzelne etwas tun. Etwa indem man beim nächsten Anflug von Erkältungsviren keine Antibiotika schluckt. Denn Antibiotika wirken gegen Bakterien, nicht aber gegen Viren – das sind völlig andere Organismen.
Autor: Irène Dietschi
Bilder: Gettyimages, Science Photo Library
Infografiken: Anne Seeger, Quellen: UZH/Prof. Roger Stephan, Interpharma, AFP, CDC, Doccheck, «Spiegel Online», «Markl Biologie» (Klett-Verlag, 2009)

6 Kommentare