Nicht ohne meine Pumpe
Ein Kunstherz ist eigentlich nur zur Überbrückung gedacht, bis ein Spenderorgan da ist. Doch einige Patienten wollen ihre Batteriepumpe nicht mehr hergeben.
Veröffentlicht am 23. Oktober 2012 - 09:20 Uhr
Als Berner Stadtpolizist trug Otto Mühlemann immer einen schweren Gurt. Allein die Pistole wog um die anderthalb Kilo. Heute schnallt der 74-Jährige wieder allerlei Geräte um: links das Handy und einen Behälter mit einer Batterie, rechts die zweite Batterie, vorn in der Tasche das Kontrollgerät. Darauf liest er den Stromverbrauch ab, den Ladezustand der Batterie und die Blutmenge, die pro Minute durch seinen Kreislauf befördert wird.

«Bis zu 300-mal täglich bücke ich mich mitsamt dem ‹Ghänk› am Bauch. Es stört mich kaum»: Otto Mühlemann, Herzpatient
Vom Kontrollgerät führt ein Kabel zur Bauchdecke und verschwindet im Innern des Körpers, gut abgedeckt von zwei sterilen Pflastern, die seine Frau alle drei Tage wechselt. Das Kabel ist mit dem Herzstück jenes Systems verbunden, das Otto Mühlemann seit zwei Jahren am Leben erhält: die Herzpumpe Heartware. Auf der linken Herzkammer eingepflanzt, pumpt sie das Blut via Hauptschlagader zurück in den Kreislauf – rund fünf Liter pro Minute, Stromverbrauch 4,7 Kilowattstunden.
Otto Mühlemann ist einer von weltweit rund 10'000 Patienten, die mit einer solchen Herzpumpe leben. «Ich musste da durch, ich hatte keine Wahl», erzählt er in breitem Berndeutsch in einem Untersuchungszimmer des Inselspitals. Dorthin kommt er regelmässig zur Kontrolle. Auch diesmal ist alles in Ordnung. Und schon erzählt er vom Schrebergarten am Wohlensee, der ihn «erhalte», von Kohlrabi, Zwiebeln und Lattich. «Bis zu 300-mal täglich bücke ich mich mitsamt dem ‹Ghänk› am Bauch. Es stört mich kaum mehr.» Und wenn er dann mal ausser Atem sei, halte er mit dem Schrebernachbarn einen Schwatz.
Mühlemann war 37 Jahre bei der Polizei, mit vielfältigen Aufgaben betraut, samt «dem Kriminellen», das ihm oft Verdruss bereitete, «doch es isch ömu ggange». Als ihm seine Frau zur Pensionierung ein Häuschen für den Schrebergarten schenkte, begann er nach Herzenslust zu gärtnern.
Damit wäre im Sommer 2010 beinahe Schluss gewesen. «Das Herz wollte nicht mehr», erzählt Mühlemann. Nicht einmal mehr hochdosierte Medikamente halfen. Bei der geringsten Bewegung geriet er ausser Atem, hatte Wasser im Körper und auf der Lunge, keinen Appetit mehr. Er kam auf die Liste für eine Herztransplantation. Aber mit 72 war es sehr unwahrscheinlich, dass ihm eines der raren Spenderorgane zugeteilt würde, sagten ihm die Ärzte offen. Denn in der Schweiz werden pro Jahr nur 30 bis 35 Herzen gespendet. 2011 starben neun Patienten auf der Herz-Warteliste.
Als Kardiologe Paul Mohacsi vorschlug, eine Herzpumpe einzupflanzen, zögerte Mühlemann nicht lange: «Entweder serble ich ab, oder ich habe eine Chance.» Er hatte eine Chance. «Es geht mir gut, und ich kann wieder alles machen wie zuvor.» Es gebe ja schliesslich noch «einen Höheren» da oben, der zu einem schaue. «Noch zehn Jahre leben, das würde mir schon gefallen.»
Wenn Paul Mohacsi, Leiter des Bereichs Herzinsuffizienz und Herztransplantation der Kardiologie an der «Insel», über seine Arbeit spricht, tauchen häufig die Begriffe «vertrauensvoll» und «verantwortungsvoll» auf. «Ich bin ein Schaffer, der für die Patienten da sein will», sagt der Kardiologe.
Für Patienten wie Otto Mühlemann, «die an einem Tiefpunkt ihres Lebens durch den Tunnel gegangen sind und einer wichtigen neuen Therapie nun die nötige Glaubwürdigkeit verleihen». Mohacsi sagt heute: «Ein Spenderherz ist nicht mehr das Mass aller Dinge.» Die Transplantation geniesse eine «Pseudoreputation», werde von «Ich schenke dir mein Herz»-Phantasien überlagert. Mit der Realität habe das wenig zu tun.
Denn die Spenderzahlen sinken seit Jahren. Ende Juni befanden sich 1064 Personen auf der Warteliste, 35 brauchten ein neues Herz. Nicht alle werden diese Wartezeit überleben. Deshalb sind Alternativen gefragt. «Anfang der neunziger Jahre hielt ich die Xenotransplantation, das Verpflanzen gentechnisch veränderter Organe von Tieren, für die vielversprechendste Technologie», sagt Mohacsi. «Einige Jahre später waren Stammzellen der Hit – und damit die Vorstellung, dass man Organe nach Belieben im Labor werde züchten können.» Auch das habe sich als Illusion erwiesen.
Im Schatten dieser biomedizinischen Hypes arbeiteten Ingenieure und Techniker an mechanischen Lösungen. Das erste totale Kunstherz, Jarvik-7, seit 1991 weltweit bei über 500 Patienten eingesetzt, galt als Wunder der Ingenieurskunst. Seine Antriebskonsole aber war ein Monstrum, das die Patienten ans Bett fesselte.
Die heutigen, miniaturisierten Systeme zielen nicht mehr darauf ab, das menschliche Herz total zu ersetzen, sondern wollen es unterstützen. Am besten bewährt haben sich «linksventrikuläre» Pumpen, solche also für die linke Herzkammer, die viel häufiger erkrankt als das «rechte Herz», das den Lungenkreislauf antreibt.
Die Modelle der dritten Generation sind technologisch so weit, dass sie eine echte Alternative zur Organtransplantation darstellen, sagt Paul Mohacsi: «Inzwischen können wir schwer herzkranken Patienten eine Therapie anbieten, die ihnen langfristig bei guter Lebensqualität das Überleben sichert.» Studien attestieren den modernen Pumpensystemen eine Zuverlässigkeit, die mit den besten Ergebnissen nach einer Herztransplantation vergleichbar ist.
In der Schweiz leiden schätzungsweise 4000 Menschen an einer schweren Herzinsuffizienz. «In vielleicht ein paar hundert Fällen helfen auch ein gesunder Lebensstil und vor allem hochwirksame Medikamente nicht mehr», sagt Mohacsi. Ein paar hundert, die – theoretisch – von einer künstlichen Herzpumpe profitieren könnten. Aufgrund der demographischen Entwicklung rechnen Spezialisten mit einer steigenden Zahl an Erkrankungen.
Bislang wurden Kunstherzen nur eingesetzt, um die Zeit bis zur Transplantation zu überbrücken; von den Krankenkassen wird bis heute nur das vergütet. Mohacsi und seine Kollegen haben sich jedoch zum Ziel gesetzt, das Kunstherz auch als Dauertherapie zu etablieren. Ein Antrag bei den Behörden ist gestellt.
Am Inselspital Bern ist es Herzchirurg Lars Englberger, der die meisten Erfahrungen mit der Implantation von Kunstherzen hat. Rein technisch, sagt der leitende Arzt, sei der Eingriff nicht extrem schwierig, vergleichbar mit einer Herzklappenoperation. Weit anspruchsvoller seien die menschlichen Aspekte. «Das sind sehr tief greifende und weitreichende Entscheidungen, die sind nicht so easy-going», sagt Englberger. Als Arzt müsse man sehr gut abwägen, wer für ein Implantat in Frage komme. Andererseits macht er die Erfahrung, dass manche Patienten ihr Kunstherz nicht mehr hergeben wollen. So auch jener Patient Anfang 50, der eines Nachts zur Transplantation aufgeboten wurde. «Der Mann lehnte ab», erzählt Englberger. «Er sagte, er lebe gut und wolle sich nicht noch einmal dem Risiko einer Herzoperation unterziehen.»

Über ein Jahr lang lebte er mit einer Pumpe, dann bekam er ein Spenderherz: Walter Kissling
Alles nicht so easy-going. Einer, der das bestätigen kann, ist Walter Kissling aus Thun. Der 65-Jährige sitzt in der Laube seines Häuschens über den Unterlagen, die seine ganze Herzgeschichte dokumentieren: ein Patientendossier, Unterlagen von Swisstransplant, Informationen über Immununterdrückung und vieles mehr, alles fein säuberlich nach Themen geordnet. Es ist die fünfte Woche nach seiner Herztransplantation. Kissling, bleiche Hände, einen ernsten Ausdruck im von Krankheit gezeichneten Gesicht, sagt: «Mein Organismus ist noch nicht auf Touren.» Körperlich sei es ihm zwar gut ergangen, sowohl vorher mit dem «Gerät» als auch jetzt mit dem Spenderherz. «Aber psychisch habe ich diese Zeit oft als Achterbahnfahrt erlebt.»
Walter Kissling war erst Mitte 30, als sich seine Herzschwäche erstmals bemerkbar machte. Der hohe Blutdruck liess sich mit Medikamenten zunächst gut einstellen. Mit 52 musste er, der schon als Kind hart hatte anpacken müssen und zuletzt als Bundesangestellter mit Leidenschaft die Wartung des Waffenplatzes Thun versah, widerwillig eine Invalidenrente beantragen. Seine Herzprobleme verschlimmerten sich weiter, mit Ende 50 bekam er einen Defibrillator gegen die Rhythmusstörungen, der auch einmal zum Einsatz kam.
Im Frühling 2011 pflanzt ihm Lars Englberger ein Kunstherz des Typs Heartmate II ein. Als er aus der Narkose erwacht, dauert es noch rund zehn Tage, bis er realisiert, was mit ihm los ist: dass ein Kabel aus seinem Bauch ragt; dass er lernen muss, alle vier bis sechs Stunden die Batterie zu wechseln; dass er keinen Puls mehr hat; dass er von jetzt an nie mehr baden, sondern nur noch duschen kann, die Konsole und Batterie in eine wasserdichte Tasche verpackt; dass er fortwährend Blutverdünner schlucken muss, weil die Oberfläche des eingepflanzten Apparates dazu neigen kann, sein Blut zu zerklumpen; dass der 300 Gramm schwere Antrieb in seinem Innern die Zeit überbrückt, bis er hoffentlich, hoffentlich ein Spenderherz bekommt.
«Ich kam gut mit dem Gerät zurecht», erzählt Walter Kissling. «Ich zeigte sogar wildfremden Leuten das Steuerungsgerät und das Kabel, wenn sie sich dafür interessierten.» Einmal sucht er nach einem Autounfall den Notfall auf – er will sichergehen, dass die Pumpe intakt ist. «Nach dem ersten Schreck machten der Notarzt und ich uns einen Spass daraus, dass die beigezogenen Medizinstudenten bei mir weder Herzschlag noch Blutdruck finden konnten.»
Was Kissling aber zunehmend Schwierigkeiten bereitet, ist die Psyche: Bleibe ich auf der Transplantationsliste? Bin ich mit bald 65 nicht zu alt für ein Spenderherz? Wann kommt der Anruf? Kommt er überhaupt? Kissling kontaktiert auch Herztransplantierte und fragt sie nach ihrem Leben mit einem Spenderherz. «Wunderbar», bekommt er unisono zu hören, so auch von einem Mann aus der Romandie, der wie er vorher mit einer künstlichen Pumpe gelebt hat. 26 Monate musste der auf die Transplantation warten.
Es dauert schliesslich 14 Monate, bis sich für Walter Kissling ein Spenderherz findet. Die ersten Tage nach der Transplantation sind für ihn ein ständiges Auf und Ab. «Als ein Arzt mich fragte, ob ich die Herzpumpe nicht vermisse, hätte ich beinahe ja gesagt. Nicht dass ich sie zurückgewollt hätte, aber sie war ein Bestandteil von mir, ich war mit ihr verwachsen.»
Auch Otto Mühlemann hat schon darüber sinniert, wie das Leben als Herztransplantierter wäre. Doch für ihn steht fest, dass er bis ans Ende seiner Tage sein Heartware behalten wird. «Selbst wenn mir ein Spenderherz angeboten würde: Ich würde nein sagen.»
Dennoch: «Um eine solche Maximaltherapie mit einem batteriebetriebenen Herz anzubieten, braucht es ein Gesamtkonzept», sagt Kardiologe Lars Englberger. «Fragen wie die nach dem sozialen Umfeld, der persönlichen Haltung des Patienten, möglichen Folgeoperationen und mehr müssen berücksichtigt werden. Das Gesamtbild ist viel komplexer als bei anderen Operationen.»
«Es hängt immer vom Einzelfall ab», bestätigt Paul Mohacsi. «Wie will man leben? Wie lange? Wie ist der Lebensplan? Was ist wichtig? Wo stehe ich? Was will ich noch erreichen? Das sind wichtige Fragen. Sie mit dem Patienten zu besprechen ist primär unsere Aufgabe.»
Und wie stirbt jemand, dessen Herzfunktion von Strom abhängt? Was ist das für ein Herztod, wenn das Pumpensystem weiter rotiert? Auch diese Fragen gehören nach Ansicht von Lars Englberger in dieses «Gesamtkonzept». «Uns fehlen die Erfahrungen, um hier schlüssige Antworten bereitzuhalten.» Man habe aber mit dem Hirntodkonzept und dem Wissen aus der Intensivmedizin die Grundlagen, um im Einzelfall vernünftig zu entscheiden. Den Tod im Detail vorzubesprechen habe aber keinen Sinn.
Auch Menschen mit Kunstherz können sterben – an Ursachen wie Blutungen im Hirn oder im Darm, Thromboembolien, Infekten, Tumoren. «In solchen Situationen kann die Pumpe weiterfunktionieren, der Mensch stirbt trotzdem», sagt Paul Mohacsi. Jeder sterbe seinen eigenen Tod. Im Übrigen sei niemand, dessen Organfunktionen von einer Maschine oder auch einem Spenderorgan übernommen worden seien, zum Leben verpflichtet. «Man bleibt ja ein Mensch, mit allen Aufs und Abs.»
Ein Gerät lasse sich, wenn es an der Zeit sei, auch abschalten.
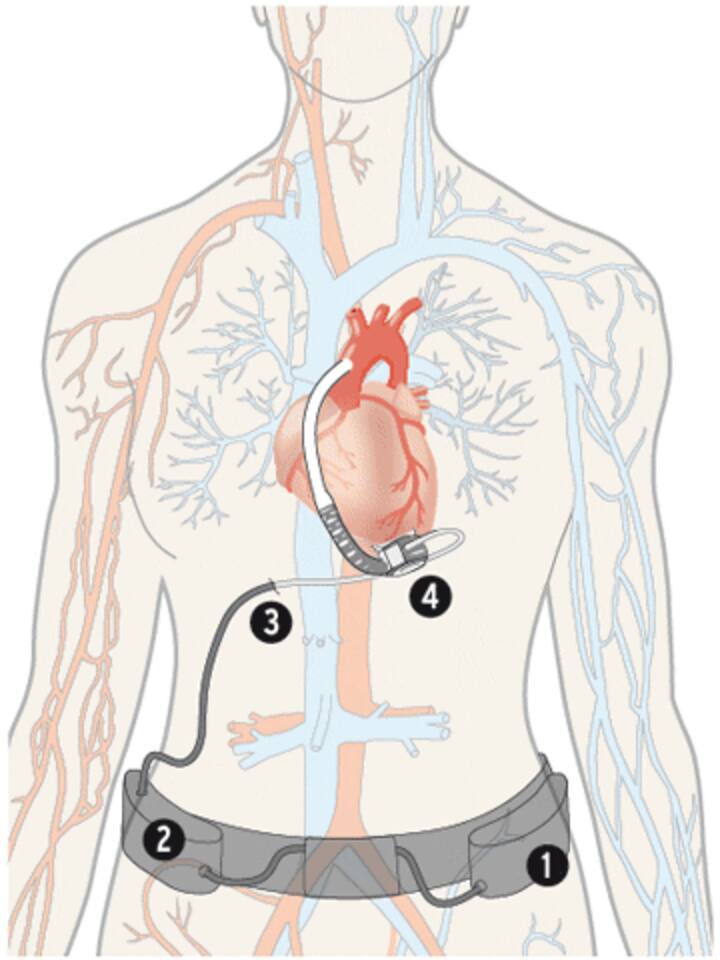
- externe Batterie
- Kontrollgerät
- Kabel durch die Bauchdecke
- Herzpumpe
Moderne Herzpumpen werden meist eingepflanzt, wenn die rechte Herzkammer noch funktioniert. Die mechanischen Pumpsysteme arbeiten nicht mit einem stossweisen, den Puls imitierenden Blutfluss, sondern transportieren einen kontinuierlichen Blutstrom. Ihre rotierenden Teile machen bis zu 15'000 Umdrehungen pro Minute. Damit sind theoretisch Blutflüsse von 8 bis 10 Litern pro Minute möglich.
Die Pumpsysteme werden auf die linke Herzkammer aufgesetzt und über aufladbare Batterien mit Energie versorgt – deren Laufzeiten betragen vier bis zwölf Stunden. Die Pumpe ist über ein Kabel durch die Bauchdecke mit einem Controller verbunden.
Derzeit forschen die Hersteller an einer weiteren Miniaturisierung. Die Batterien sollen in den Körper implantiert werden können –und berührungslos per Induktion aufgeladen werden. Das lästige Kabel und damit eine häufige Infektionsquelle sollen dann wegfallen, die Bewegungsfreiheit mit der Herzpumpe soll praktisch grenzenlos sein.
Quellen: Thoratec, «Tages-Anzeiger»; Infografik: Beobachter/mt
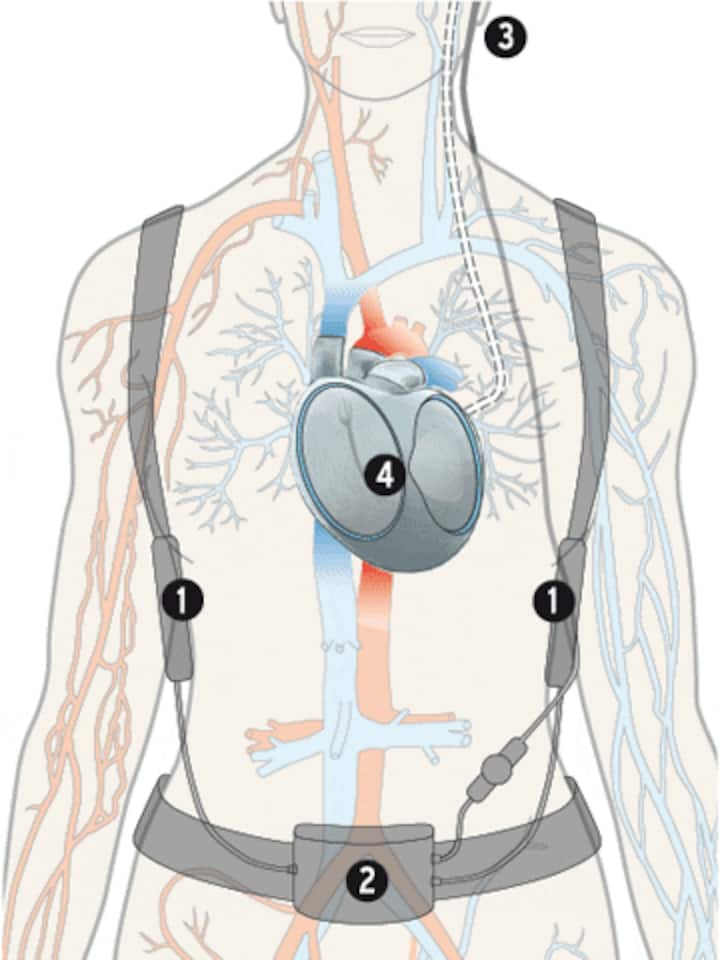
- externe Batterien
- Kontrollgerät
- Eintritt zum implantierten Kabel (hinter dem Ohr)
- Kunstherz
Falls beide Herzkammern nur noch eingeschränkt funktionieren, kann ein sogenanntes komplettes Kunstherz eingesetzt werden. Es bildet die natürliche, pulsierende Pumpfunktion mechanisch nach. Dabei pressen bewegliche Membrane das Blut in die Gefässe des Körperkreislaufs und des Lungenkreislaufs. Komplette Kunstherzen konnten sich als Dauerlösung bisher nicht durchsetzen – die Technologie ist trotz jahrzehntelanger Entwicklungsarbeit zu komplex.
Quellen: Carmat, «Tages-Anzeiger»; Infografik: Beobachter/mt
Dank technischen Fortschritten gibt es immer mehr Möglichkeiten, Organfunktionen des menschlichen Körpers maschinell zu ersetzen. Manche Systeme werden nur für kurze Zeit eingesetzt, andere sind für Dauerbetrieb konzipiert. Beispiele:
- Herz-Lungen-Maschine: kann die Pumpfunktion des Herzens sowie die Lungenfunktion für einen beschränkten Zeitraum (während einer Operation) ersetzen.
- Beatmungsgerät: elektrisch gesteuert oder pneumatisch angetrieben, zur Beatmung von Personen mit unzureichender oder ausgesetzter Eigenatmung.
- Cochlea-Implantat: Hörprothese für Gehörlose, deren Hörnerv noch funktioniert. Dabei werden Elektroden in die Cochlea (Hörschnecke) eingepflanzt.
- Hämodialyse: ein Blutreinigungsverfahren, das bei Nierenversagen als Ersatz zum Einsatz kommt.
- Myoelektrische Prothesen: Ersatzglieder der neuen Bauart, die die elektrische Spannung auf der Haut des amputierten Stumpfes nutzen und mit einem Fremdantrieb funktionieren.
- Hirn-Maschinen-Schnittstellen: Verknüpfung von Hirnsignalen mit Geräten, so dass zum Beispiel Tetraplegiker einen Rollstuhl steuern können.
- Herzpumpe oder Kunstherz: Implantate für Patienten, die an unheilbaren Herzerkrankungen leiden.
